This post is also available in: Persian English
Եթե մենք պետք է ընտրեինք միացրած տարր՝ որպես աէրոբ կյանքի խորհրդանիշ, թթվածինը անշուշտ կհաղթի ցուցակում։ Երկրի մթնոլորտի մոտ 21%-ը բաղկացած է թթվածնից, և այս տարրը հիմնարար դեր է խաղացել կենսաբանական էվոլյուցիայի ձևավորման մեջ։ Երկրի մթնոլորտում թթվածնի հայտնվելը մոտ 2,4 միլիարդ տարի առաջ՝ «Մեծ օքսիդացման իրադարձության» ընթացքում, հիմքովին փոխեց կյանքի էվոլյուցիայի ընթացքը։ Օրգանիզմները, որոնք կարող էին օգտագործել թթվածինը էներգիայի արտադրության համար, ստացան էվոլյուցիոն առավելություն՝ աէրոբ նյութափոխանակության բարձր արդյունավետության շնորհիվ համեմատած անաերոբ ուղիների հետ։
Մարդկանց մոտ գրեթե յուրաքանչյուր բջիջը կախված է թթվածնից գոյատևման համար։ Թթվածնի մատակարարման ընդհատումը նույնիսկ մի քանի րոպե կարող է հանգեցնել բջիջների մահվան և անշրջելի հյուսվածքային վնասների, հատկապես էներգիայի բարձր պահանջ ունեցող հյուսվածքներում, ինչպես գլխուղեղը և սիրտը։ Բայց հենց այն թթվածինը, որը կենսունակության համար անհրաժեշտ է, մոլեկուլյար մակարդակում կարող է դառնալ վնասակար գործոն։
Այս կենսաբանական պարադոքսը՝ թթվածինը որպես կյանքի աղբյուր և հնարավոր վնաս պատճառող գործոն, բջջային և մոլեկուլյար կենսաբանության ամենահետաքրքիր թեմաներից մեկն է։ Այս երկակիությունը հասկանալը կարևոր է ոչ միայն բժշկության և բիոտեխնոլոգիայի համար, այլև արդյունաբերական ոլորտների, որոնք զբաղվում են թթվածնի արտադրությամբ, պահպանումով և տեղափոխմամբ, քանի որ թթվածնի որակը, մաքրությունը և վերահսկումը կարող են խորապես ազդել կենդանի համակարգերի վրա։
Թթվածինը և բջջային նյութափոխանակությունը՝ կյանքի շարժիչը
1. Բջջային շնչառություն՝ գլյուկոզայից ATP
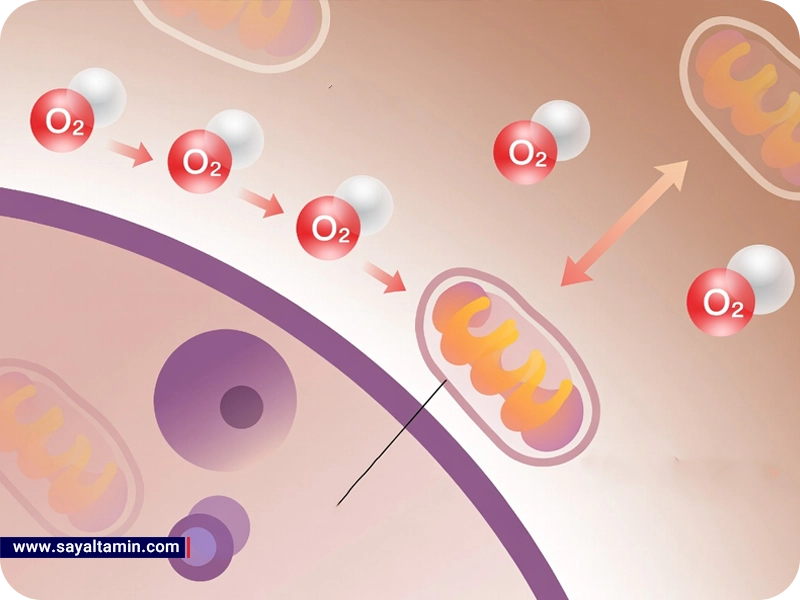
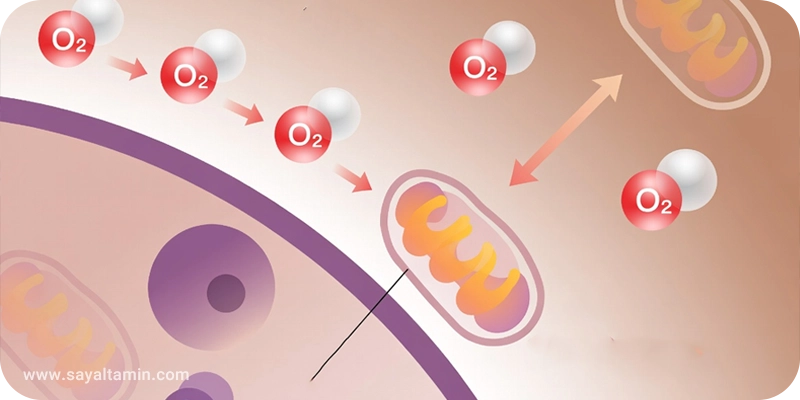
Թթվածնի դերը նյութափոխանակությունում հասկանալու համար պետք է դիտարկել բջջի էներգիայի արտադրության ուղիները։ Բջջային շնչառությունը բազմափուլ գործընթաց է, որի ընթացքում օրգանական մոլեկուլներում (օր.՝ գլյուկոզա) պահպանված քիմիական էներգիան փոխակերպվում է ATP-ում։ Այս գործընթացը ներառում է երեք հիմնական փուլեր։
- Գլիկոլիզ (ցիտոպլազմայում)
- Կրեբսի ցիկլ կամ սիտրիկ թթվի ցիկլ (միտոխոնդրիայում)
- Էլեկտրոնների տեղափոխման շղթա և օքսիդատիվ ֆոսֆորիլացում (միտոխոնդրիայի ներքին թաղանթում)
Առաջին երկու փուլերում բարձր էներգիայի էլեկտրոնները դուրս են բերվում վառելիքի մոլեկուլներից և փոխանցվում NADH և FADH₂ տեղափոխողներին։ Բայց մեծաքանակ ATP արտադրության վճռորոշ քայլը էլեկտրոնների տեղափոխման շղթան է, որտեղ թթվածինը կենտրոնական դեր ունի։
2.Թթվածինը որպես վերջին էլեկտրոն ընդունող
Էլեկտրոնների տեղափոխման շղթայում էլեկտրոնները անցնում են բազմաթիվ մեմբրանային պրոտեինային համալիրներով։ Շղթայի վերջում թթվածինը ծառայում է որպես վերջին էլեկտրոն ընդունող, միանալով էլեկտրոններին և պրոտոններին՝ ջուր առաջացնելով․
O2+4e−+4H+→2H2OO_2 + 4e^- + 4H^+ → 2H_2OO2+4e−+4H+→2H2O
Այս պարզ թվացող ռեակցիան կարևոր է բջջի գոյատևման համար։ Թթվածնի բացակայության դեպքում էլեկտրոնների շղթան կանգնում է, և ATP արտադրությունը զգալիորեն նվազում է։ Նման պայմաններում բջիջները անցնում են անաերոբ ուղիների, ինչպես ֆերմենտացիան, որոնք շատ ավելի քիչ էներգաարդյունավետ են։
Մոտավորապես, մեկ գլյուկոզայի ամբողջական աէրոբ նյութափոխանակությունը կարող է արտադրել մոտ 30–32 ATP մոլեկուլ, մինչդեռ անաերոբ պայմաններում ստացվում է միայն մոտ 2 ATP։ Այս տարբերությունը ընդգծում է թթվածնի կենսաբանական կարևորությունը։
3.Միտոխոնդրիա՝ էներգիայի աղբյուր և հնարավոր վնասի աղբյուր
Միտոխոնդրիան հաճախ կոչվում է «բջջային էներգետիկ կենտրոն», բայց էներգիայի արտադրության հետ միասին այն հանդիսանում է ռեակտիվ թթվածնի տեսակների (ROS) հիմնական աղբյուրը։ Կոնկրետ պայմաններում, էլեկտրոնների շղթայում օգտագործվող թթվածնի մոտ 1–2%-ը ամբողջովին չի վերածվում ջրի, փոխարենը ձևավորում է մասնակիորեն նվազեցված տեսակներ, ինչպիսիք են սուպերօքսիդը (O₂•⁻)։
Ֆիզիոլոգիական պայմաններում այս փոքր քանակության ROS-ը վնասակար չէ և նույնիսկ մասնակցում է բջջային ազդանշանների կարգավորմանը։ Սակայն, եթե ROS-ի արտադրությունը ավելանա կամ բջջային պաշտպանական համակարգերը թույլանան, արտադրության և չեզոքացման հավասարակշռությունը խախտվում է, առաջացնելով օքսիդատիվ սթրես։
Թթվածնի երկրորդ կողմը՝ կենսաբանական ազդանշանից օքսիդատիվ սթրես
Մոլեկուլյար թթվածինը (O₂) իր հիմնական վիճակում համեմատաբար կայուն է, սակայն իր եզակի էլեկտրոնային կոնֆիգուրացիայի պատճառով (երկու զուգորդված էլեկտրոններ առանձին օրբիտալներում) այն հեշտությամբ մասնակցում է ռեդոքս ռեակցիաներին որոշակի պայմաններում։ Այս հատկությունը թույլ է տալիս կենսաբանական վառելիքներից էներգիա հանելը, ինչպես նաև ռեակտիվ և հնարավոր վնասակար փոխառաջացումների ձևավորումը։
Բջջում թթվածինը երբեք միայն թեակային գազ չէ՝ այն մասնակցում է էլեկտրոնների բարդ փոխանակումների ցանցին։ Այս դինամիկ միջավայրում որոշ թթվածին ամբողջությամբ չի վերածվում ջրի և ձևավորում է ռեակտիվ թթվածնի տեսակներ (ROS)։
ROS՝ աէրոբ նյութափոխանակության անխուսափելի հետևանք
ROS արտադրությունը ոչ թե կենսաբանական սխալ է, այլ բնական և անխուսափելի արդյունք՝ թթվածնի օգտագործման որպես վերջին էլեկտրոն ընդունող։ Միտոխոնդրիայում, որտեղ էլեկտրոնների շղթան աշխատում է ATP արտադրելու համար, էլեկտրոնները անցնում են պրոտեինային համալիրներով։ Մինչև վերջնական արդյունավետությունը բարձր է, գործընթացը երբեք ամբողջովին չի ավարտվում։
Էլեկտրոնների փոքր մասն արձագանքում է թթվածնի հետ, առաջացնելով սուպերօքսիդ։ Չնայած այս փոքր մասնիկը միայն 1–2%-ն է ընդհանուր օգտագործվող թթվածնից, պետք է նկատի ունենալ, որ յուրաքանչյուր բջիջ օրական օգտագործում է միլիարդավոր թթվածնի մոլեկուլներ, այդ փոքր մասնիկը վերածվում է մեծ թվով ռեակտիվ մոլեկուլների։
Սուպերօքսիդը կարող է վերածվել ջրածնի պերօքսիդի, և երկաթի նման մետաղների առկայության դեպքում կարող է առաջացնել հիդրոքսիլ ռադիկալներ՝ ամենաազդեցիկ քիմիական վնասը պատճառող կենսաբանական տեսակներ։ Այս շղթան ցույց է տալիս աէրոբ նյութափոխանակության ներքին ռիսկերը։
ROS-ի կարգավորման դեր՝ հին հասկացությունը վերանայելով
Տասնամյակներ ROS-ը դիտվում էր միայն որպես վնասակար նյութափոխանակության կողմնակի արտադրանք։ Սակայն վերջին 20 տարում հետազոտությունները ցույց են տվել, որ բջիջները օգտագործում են ROS որպես ազդանշանային մոլեկուլներ։
Ջրածնի պերօքսիդը միայն վնասակար օքսիդանտ չէ, այն կարող է ռիվերսիբլ օքսիդացնել տիոլ խմբերը պրոտեիններում՝ կարգավորելով դրանց ակտիվությունը։ Շատ ազդանշանային ուղիներ՝ աճը, տարբերակումն, սթրեսի պատասխանները և նույնիսկ էներգիայի նյութափոխանակությունը, զգայուն են ROS-ի նուրբ տատանումներին։
Բջիջները սովորել են «կառավարվող վտանգը» օգտագործել որպես կարգավորման գործիք, երբ օքսիդացման և նվազեցման հավասարակշռությունը դառնում է բջջային հաղորդակցության լեզվի մաս։ Սակայն ինչպես ցանկացած ազդանշանային համակարգում, ճշգրտությունը կարևոր է՝ օգտակար և վնասակար ազդեցությունների միջև սահմանը նեղ է։
Հավասարակշռության խախտում՝ օքսիդատիվ սթրես
Առողջ բջիջներում ROS արտադրությունն ու չեզոքացումը դինամիկորեն հավասարակշռված են։ Էնզիմատիկ և ոչ էնզիմատիկ հակաօքսիդանտ համակարգերը մշտապես ճնշում են ռեակտիվ տեսակները։ Սակայն, եթե հավասարակշռությունը խախտվի՝ էներգիայի պահանջի աճի, քրոնիկական բորբոքման, շրջակա միջավայրի թունավոր նյութերի, միտոխոնդրիալ ֆունկցիայի խախտման կամ պաշտպանական համակարգերի թուլացման պատճառով, առաջանում է օքսիդատիվ սթրես։
Օքսիդատիվ սթրեսը միայն ROS-ի քանակի ավելացում չէ, այն ցույց է տալիս կենսաբանական համակարգի անկարողությունը՝ կառավարել դրանց հետևանքները։ Այս վիճակում էական բջջային մոլեկուլները դառնում են օքսիդատիվ ռեակցիաների թիրախ։
Լիպիդները՝ հարուստ անսարսափած ճարպային թթուներով, բարձրապես խոցելի են ռադիկալային հարձակման համար։ Լիպիդների պերօքսիդացումը կարող է փոխել թաղանթների կառուցվածքն ու հեղուկությունը, խանգարել իոնային ջրանցքները և նույնիսկ ակտիվացնել բջջի մահվան ազդանշանները։ Գլխուղեղի նման ճարպային հարուստ հյուսվածքներում վնասը հատկապես զգալի է։
Պրոտեիններն էլ խոցելի են։ Օքսիդացումը կարող է խանգարել նրանց եռաչափ կառուցվածքը, վնասելով գործառույթը։ Վնասված պրոտեինները կարող են կուտակվել լուծելի չլինող կառուցվածքներում, ինչը դիտվում է նեյրոդեգեներատիվ հիվանդություններում՝ օրինակ Ալցհեյմերի դեպքում։
Միգուցե ամենակարևորն այն է, որ ROS-ը թիրախավորում է նաև գենետիկական նյութը։
ԴՆԹ՝ օքսիդատիվ հարձակման ներքո
Նուկլեար և միտոխոնդրիալ DNA-ն շարունակաբար ենթարկվում է օքսիդատիվ վնասներին։ Արյան հիմքերի քիմիական փոփոխությունները, մեկ և երկու շղթայական ընդհատումները, ու կետային մուտացիաները դրանց հետևանքներից են։
Չնայած DNA-ի վերականգնման համակարգերի առկայությանը, մեխանիզմները կատարյալ չեն։ Ժամանակի ընթացքում վնասները կուտակվում են, և այս աստիճանական կուտակումը հիմք է հանդիսանում այն տեսությունների համար, որոնք կապում են մոլեկուլյար վնասը ծերացման հետ։
Միտոխոնդրիալ DNA-ն (mtDNA) հատկապես խոցելի է։ Փոքր և շրջանաձև mtDNA-ն գտնվում է ROS արտադրության վայրերի մոտ և չունի նուկլեար DNA-ի լայնածավալ հիստոնային պաշտպանությունը։ mtDNA-ի վնասը կարող է խանգարել էլեկտրոնների շղթայի արդյունավետությունը, ավելացնել ROS արտադրությունը և ստեղծել բացասական հակադարձ կապ՝ բացատրելով բջջային ֆունկցիայի տարիքային նվազումը։
Աղյուսակ 2 – ROS-ի ֆունկցիոնալ սպեկտր՝ կարգավորումից մինչև վնաս
| ROS-ի մակարդակ | Ֆիզիոլոգիական վիճակ | Կենսաբանական արդյունք |
|---|---|---|
| Շատ ցածր | Նորմալ ազդանշում | Աճի և տարբերակման կարգավորում |
| Միջին, վերահսկված | Ստորին ռեդոքս հավասարակշռություն | Նորմալ նյութափոխանակություն |
| Բարձր, շարունակական | Օքսիդատիվ սթրես | Լիպիդների և պրոտեինների վնաս |
| Շատ բարձր | Բջջային կոլապս | Ապոպտոզ կամ նեկրոզ |
Թթվածինը, բորբոքումը և համակարգային ծերացում
Ավելին, ROS կարող է ակտիվացնել բորբոքային ուղիներ։ Քրոնիկ, ցածր մակարդակի բորբոքային ակտիվացումը առաջացնում է այն վիճակը, որը որոշ հետազոտողներ անվանում են inflammaging։
Այս վիճակը առաջացնում է իմունային համակարգի շարունակական ակտիվացման ցիկլ։ Կայուն, թեթև բորբոքումը կարող է նպաստել տարիքային հիվանդություններին, այդ թվում՝ սրտանոթային հիվանդություններ, 2-րդ տիպի շաքարախտ և նյարդաբանական խանգարումներ։
Ուստի, թթվածինը ազդում է ոչ միայն բջջային, այլև համակարգային ծերացման գործընթացների վրա։
Թթվածին, Օքսիդատիվ Սթրեսը և Կենսաբանական Տարիքի Թերորիաները
Տարիքը՝ գենետիկորեն ծրագրավորված՞, թե վնասների կուտակում։
Տարիքը բազմաչափ երևույթ է և վերջնական պատասխան չունի։ Արդյոք դա նախապես որոշված գենետիկական ծրագրի արդյունք է, թե՞ մոլեկուլյար վնասների ժամանակի ընթացքում կուտակման հետևանք։ Ընդհանուր տեսությունների մեջ ամենահզորներից մեկը տարիքային ազատ ռադիկալների տեսությունն է, որը անմիջապես կապում է թթվածնի երկակի դերին։
1950-ականներին Դենհեմ Հարմանը առաջարկեց, որ աէրոբ նյութափոխանակության ընթացքում ազատ ռադիկալների շարունակական արտադրությունը աստիճանաբար վնասում է բջջային բաղադրիչները, և այդ վնասների կուտակումը կազմում է տարիքային գործընթացների կենսաբանական հիմքը։ Այս տեսությունը հեղափոխական էր՝ առաջին անգամ անմիջապես կապելով էներգիայի նյութափոխանակությունը տարիքային գործընթացների հետ։
Այս մոտեցման համաձայն, որքան շատ է օրգանիզմը օգտագործում թթվածին, այնքան ավելի շատ ազատ ռադիկալներ են արտադրվում, արագացնելով վնասների կուտակումը։ Կարող ենք ասել՝ «շնչառության արժեքը» կյանքի արժեքն է։
Բայց կենսաբանական գիտությունը երբեք կանգ չի առնում։
Ազատ ռադիկալների տեսության վերանայում
Վերջին տասնամյակներում փորձարարական տվյալները դարձել են ավելի բարդ, քան սկզբնական պարզ տեսությունը կարող էր ընդգրկել։ Բարձր նյութափոխանակության մակարդակ ունեցող որոշ օրգանիզմներ ապրել են զարմանալի երկար։ Արևադարձային կենդանիների որոշ մոդելներում բարձր հակաօքսիդանտ մակարդակները երկար կյանք չէին ապահովում։ Որոշ դեպքերում, նույնիսկ ROS-ի թեթև ավելացումները կապ են ունեցել կյանքի երկարացման հետ։
Այս հայտնագործությունները ցույց տվեցին, որ ROS-ը պարզապես «համաձայնի թունավոր նյութեր» չեն, այլ կյանքի կարգավորման ցանցի հիմնական բաղադրիչներ։ Արդյունքում, դասական ազատ ռադիկալների տեսությունը զարգացավ դեպի ավելի ժամանակակից տարբերակներ՝ ընդգծելով «ռեդոքս հավասարակշռության խախտումը» և «հարմարվողական սթրեսային ազդանշանները»։
Հիմնական հասկացություն, որն առաջացել է այս վերանայումից, հայտնի է որպես հորմեզ։
Հորմեզ՝ երբ թեթև սթրեսը դառնում է օգտակար
Հորմեզը վերաբերում է երևույթի, երբ ցածր մակարդակի սթրեսային գործոնի ազդեցությունը ակտիվացնում է պաշտպանական ուղիները և վերջիվերջո բարձրացնում բջջային դիմադրողականությունը։ Թթվածնի համատեքստում, ROS-ի թեթև և վերահսկված աճը կարող է ակտիվացնել պաշտպանական մեխանիզմներ։
Օրինակներ՝
- Nrf2 տրանսկրիպցիոն գործոնի ակտիվացում՝ հակաօքսիդանտ գեների արտահայտությունն ավելացնելով
- DNA-ի վերականգնման ուղիների ակտիվացում
- Միտոխոնդրիայի արդյունավետության բարձրացում
Այսպիսով, ROS-ի ցածր մակարդակները կարող են ծառայել որպես «չափանիշային ազդանշան», ամրապնդելով բջջային պաշտպանական համակարգերը։ Սակայն քրոնիկ կամ չափազանց սթրեսը կարող է գերազանցել այդ պաշտպանությունը, առաջացնելով գերիշխող բջջային վնաս։
Այս մոտեցումը ցույց է տալիս, որ թթվածնի և տարիքայնացման հարաբերությունը ուղիղ կամ պարզ չէ՝ այն կախված է ինտենսիվությունից, տևողությունից և կենսաբանական համատեքստից։
Միտոխոնդրիա՝ տարիքայնացման հավասարման կենտրոնում
Մոտ բոլոր ժամանակակից տարիքային մոդելները միտոխոնդրիային կենտրոնում են տեղադրում՝ լոգիկական է՝ դրանք հիմնական էներգիայի աղբյուրն ու ROS արտադրող հիմնական օղակն են։
Տարիքի հետ նկատվում են հետևյալ միտոխոնդրիալ փոփոխությունները՝
- Էլեկտրոնների տեղափոխման շղթայի արդյունավետության անկում
- Էլեկտրոնների արտահոսքի աճ
- Միտոխոնդրիալ DNA-ում (mtDNA) մուտացիաների կուտակում
- ATP-ի արտադրության նվազեցված կարողություն
Այս փոփոխությունները կարող են ձևավորել շրջադարձային ցիկլ՝ միտոխոնդրիալ դիսֆունկցիա → ROS-ի աճ → հետագա վնաս → ավելի մեծ դիսֆունկցիա։
Բայց որոշ ուսումնասիրություններ ցույց են տվել, որ կյանքի վաղ փուլում թեթև ROS աճը կարող է ակտիվացնել երկար կյանք ապահովող ուղիները, ինչը ցույց է տալիս, որ օքսիդատիվ ազդանշանների որակը ավելի կարևոր է, քան միայն ROS քանակը։
Կալորիական սահմանափակում՝ թթվածնի օգտագործման նվազեցում կամ օպտիմիզացում
Կենսաբանական երկար կյանք ապահովելու ամենահզոր միջամտություններից մեկը կենդանիների մոդելներում կալորիական սահմանափակումն է առանց թերսնումի։ Այս միջամտությունը ուսումնասիրվել է 1930-ականներից և երկարացրել կյանքի տևողությունը՝ ճ Yeast-ից մինչև երկկենցաղներ և կաթնասուններ։
Սկզբնական ենթադրությունները ենթադրում էին, որ կալորիական սահմանափակումը նվազեցնում է նյութափոխանակությունը և թթվածնի օգտագործումը, հետևաբար նվազեցնում ROS արտադրությունը։ Ավելի մանրամասն ուսումնասիրությունները ցույց տվեցին ավելի բարդ պատկեր։
Կալորիական սահմանափակումը ակտիվացնում է կոնկրետ մոլեկուլյար ուղիներ՝
- Սիրտիններ (հատկապես SIRT1)
- AMPK
- mTOR-ի արգելափակում
Այս ուղիները բարելավում են միտոխոնդրիայի արդյունավետությունը, բարձրացնում ավտոֆագիան (վնասված բաղադրիչների հեռացում) և ամրացնում բջջային դիմադրողականությունը։ Արդյունքում, կալորիական սահմանափակումը ոչ միայն կարգավորում է թթվածնի օգտագործումը, այլև օպտիմիզացնում է դրա արդյունավետությունը։
Մասնավորապես, հիմնական հարցը կարող է լինել ոչ թե «Որքան թթվածին ենք օգտագործում», այլ՝ «Ինչպես ենք այն օգտագործում»։
Աղյուսակ 3 – Մոլեկուլյար ուղիներ, ROS և տարիքայնացում
| Մոլեկուլյար Ուղի | ROS Կապը | Տարիքի վրա ազդեցություն |
|---|---|---|
| Nrf2 | Թեթև ROS-ով ակտիվացված | Հակաօքսիդանտ գեների արտահայտման բարձրացում |
| SIRT1 | Էներգիայի կախված | DNA-ի վերականգնում և միտոխոնդրիայի արդյունավետության բարձրացում |
| AMPK | Էներգիայի սենսոր | Առաջարկում է արդյունավետ նյութափոխանակություն |
| mTOR | Սննդային զգայուն | Արգելափակումը կապում է կյանքի երկարացման հետ |
| p53 | DNA-ի վնասի պատասխան | Կարգավորում է բջջային մահը և բջջային տարիքայնացումը |
Բջջային սենեսցեն և թթվածին
Թթվածնի և տարիքայնացման մյուս կարևոր ասպեկտը բջջային սենեսցեն է։ Այս վիճակում բջիջները դուրս են գալիս բաշխման ցիկլից կուտակված վնասների պատճառով՝ ներառյալ օքսիդատիվ վնասը, բայց մնում են կենդանի։ Այս բջիջները հաճախ արտազատում են բորբոքային մոլեկուլների մի շարք, որոնք փոխում են հյուսվածքային միջավայրը։
Սենեսցենտ բջիջների կուտակումն հյուսվածքներում տարիքայնացման նշան է։ Քրոնիկ օքսիդատիվ սթրեսը հիմնական գործոններից մեկն է, որը բջիջները հասցնում է այս վիճակին։
Հակաօքսիդանտ համակարգեր և ռեդոքս հավասարակշռության պահպանություն
Ինչպե՞ս են բջիջները ապրում թթվածնի հետ առանց վնասվելու
Եթե թթվածինը դիտվում է որպես վերահսկվող կրակ, որը սնուցում է կյանքը, ապա հակաօքսիդանտ համակարգերը ծառայում են որպես ճարտարապետական մեխանիզմներ՝ կանխելու այդ կրակի անհսկող տարածումը։ Աէրոբ կյանքը անհնար կլիներ առանց այս պաշտպանիչ համակարգերի։ Իրականում, բազմաբջջային էվոլյուցիան տեղի է ունեցել օքսիդացիայից ստացված էներգիայի կառավարման մեխանիզմների հետ միասին։
Բջիջները մշտապես ենթարկվում են ռեդոքս ռեակցիաների միտոխոնդրիայում, ցիտոզոլում, նուկլեուսում, էնդոպլազմատիկ ցանցում և պլազմային թաղանթում։ Ռեդոքս հավասարակշռության պահպանումը, հետևաբար, դինամիկ, տեղային և պահ առ պահ գործընթաց է, ոչ թե ստատիկ վիճակ։
Պաշտպանության առաջին գիծը՝ հակաօքսիդանտ էնզիմներ
Բջջային պաշտպանական համակարգի հիմքում էնզիմներն են, որոնք նախատեսված են ROS-ը չեզոքացնելու համար։ Դրանք ռազմավարական տեղադրված են և ունեն արագ ռեակցիայի կինետիկա։
- Սուպերօքսիդ դիսմուտազ (SOD)՝ փոխակերպում է սուպերօքսիդը ջրածնի պերօքսիդի, որը ավելի կայուն և վերահսկելի է։ Բջիջները ունեն բազմաթիվ SOD իզոֆորմեր՝ ցիտոզոլային, միտոխոնդրիալ և էքստրասելյուլյար։
- Ջրածնի պերօքսիդը հետագայում քայքայվում է կատալազ և գլուտաթիոն պերօքսիդազ միջոցով։ Կատալազը այն անմիջապես ջուր և թթվածին է վերածում, իսկ գլուտաթիոն պերօքսիդազը օգտագործում է գլուտաթիոն՝ այն ջրի վերածելու համար։
Այս շղթան ցույց է տալիս, որ մարմինը միայն չի հեռացնում ROS-ը, այլ կառավարում է դրանք վերահսկված, քայլ առ քայլ ձևով։
Գլուտաթիոն՝ ռեդոքս հավասարակշռության հիմքը
Բջջային հակաօքսիդանտների մեջ գլուտաթիոնը հատկապես կարևոր է։ Այս փոքր տրիպեպտիդը գոյություն ունի նվազեցված (GSH) և օքսիդացված (GSSG) ձևերով։ GSH-ի և GSSG-ի հարաբերակցությունը բջջային ռեդոքս վիճակի հիմնական ցուցիչն է։ ROS-ի աճի դեպքում GSH-ն սպառվում է։ Եթե բջիջը չի կարող վերականգնել այն, ռեդոքս հավասարակշռությունը թեքվում է դեպի օքսիդատիվ սթրես։
Տարիքի հետ, գլուտաթիոնի մակարդակները նվազում են բազմաթիվ հյուսվածքներում, նպաստելով ծեր տարեցների օքսիդատիվ վնասների նկատմամբ զգայունության աճին։
Ինչու հակաօքսիդանտ հավելումները միշտ չէ, որ հրաշագործ են
Տասնամյակների ընթացքում մտածում էին, որ հակաօքսիդանտ հավելումների, ինչպես C վիտամին, E վիտամին կամ բետա-կարոտին, օգտագործումը կարող է դանդաղեցնել տարիքայնացումը։ Մեծ կլինիկական փորձարկումները սակայն ցույց տվեցին ավելի բարդ պատկեր։
Բարձր դոզաներով հակաօքսիդանտ հավելումները հաճախ չէին երկարացնում կյանքը և որոշ դեպքերում բարձրացրին որոշ հիվանդությունների ռիսկը։
Հիմնավորումը հորմեզն է՝ եթե ROS-ը ծառայում է ազդանշանային դերերի, ապա չափազանց շատ հեռացնելը կարող է խափանել հարմարվողական ուղիները։ Մարմինը պահանջում է որոշակի մակարդակի օքսիդատիվ ակտիվություն՝ ռեդոքս հոմեոստազը պահպանելու համար։ Ամբողջական ճնշումը ոչ հնարավոր է, ոչ ցանկալի։
Ռեդոքս հոմեոստազը՝ տարիքայնացման կենտրոնական հասկացությունը
Ռեդոքս հոմեոստազը վերաբերում է օքսիդացման և նվազեցման ռեակցիաների դինամիկ հավասարակշռությանը բջջում՝ որպես կենսաբանական տերմոստատ։ Չէ թե չափազանց օքսիդացումը, ոչ էլ չափազանց նվազեցումը օպտիմալ չեն։
Տարիքի հետ, այս կենսաբանական տերմոստատը ձախողվում է՝ միտոխոնդրիայի արդյունավետությունը նվազում է, վերականգնման համակարգերը թուլանում, գլուտաթիոնի մակարդակները նվազում և բորբոքային պատասխանները աճում են։ Արդյունքը աստիճանաբար շարժվում է քրոնիկ օքսիդատիվ վիճակների ուղղությամբ։
Թթվածինը դեռ անհրաժեշտ է կյանքի համար, բայց համակարգի կարողությունը կառավարել դրա հետևանքները նվազում է՝ բացատրելով, թե ինչու տարիքային հիվանդություններին հաճախ ուղեկցում են բարձրացված օքսիդատիվ սթրեսի նշաններ։
Օքսիդատիվ սթրես, թթվածին և տարիքի հետ կապված հիվանդություններ
Երբ ռեդոքս անհավասարակշռությունը ազդում է հյուսվածքների և ամբողջ օրգանիզմի վրա։
Մինչ այժմ թթվածինը դիտվել է բջջային մակարդակում՝ միտոխոնդրիայում, DNA-ում, ազդանշանային ցանցերում և պաշտպանական համակարգերում։ Սակայն ռեդոքս անհավասարակշռության հետևանքները անցնում են մեկ բջիջից և դառնում համակարգային երևույթ՝ հատկապես տարիքի հետ։
Քրոնիկ ROS կուտակումը և պաշտպանական կարողության նվազումը ստեղծում է միջավայր, որը նպաստում է տարիքային հիվանդությունների զարգացմանը։ Այս պայմանները չեն առաջանում «չափից շատ թթվածնի» պատճառով, այլ կենսաբանական համակարգերի անկարողության հետևանքով շարունակաբար կառավարել դրա օգտագործումը։
Սիրտանոթային հիվանդություններ՝ անոթների օքսիդացում
Օքսիդատիվ սթրեսի հայտնի օրինակ է աթերոսկլերոզը։ Անոթների պատերին ցածր խտությամբ լիպոպրոտեինները (LDL) օքսիդացվում են։ Օքսիդացված LDL-ը ճանաչվում և ներծծվում է իմունային բջիջների կողմից՝ ի վերջո ձևավորելով բլոկներ անոթի պատում։
ROS-ը կարևոր դեր է խաղում՝ միջնորդելով LDL օքսիդացումը և ակտիվացնելով բորբոքային ուղիները։ Արդյունքը անոթների ճկունության նվազումն է, զարկերակների նեղացումը և սրտի գրոհի կամ ինսուլտի ռիսկի ավելացումը։
Անոթների լորձաթաղանթային բջիջներն էլ զգում են օքսիդատիվ սթրեսը տարիքի հետ։ Նիտրիկ օքսիդի արտադրությունը՝ կարևոր անոթների լայնացման համար, նվազում է, խախտելով արյան ճնշման կարգավորումը։ Այս օքսիդատիվ միջնորդների միջոցով թթվածինը դառնում է հիմնական մարտահրավեր տարեցների սիրտանոթային առողջության համար։
Տիպ 2 շաքարային դիաբետ՝ նյութափոխանակության և ROS-ի վիրուսային ցիկլ
Տիպ 2 շաքարային դիաբետում ինսուլինի նկատմամբ դիմադրությունը և գլյուկոզայի նյութափոխանակության խանգարումը ուղեկցվում են ROS-ի արտադրության բարձրացմամբ։ Արյան գլյուկոզայի բարձր մակարդակը բարձրացնում է էլեկտրոնների հոսքը էլեկտրոնային տեղափոխման շղթայում՝ ուժեղացնելով էլեկտրոնների արտահոսքն ու սուպերօքսիդի արտադրությունը։
ROS-ը, իր հերթին, ուժեղացնում է բորբոքային ուղիները և խանգարում ինսուլինի ազդանշանները, ստեղծելով վիրուսային ցիկլ՝ հիպերգլիկեմիա → ROS-ի բարձրացում → ինսուլինի դիմադրության ուժեղացում → հիպերգլիկեմիայի հետագա աճ։
Ժամանակի ընթացքում շաքարախտի ընթացքում օքսիդատիվ սթրեսը վնասում է միկրովարիկուլյատուրան, երիկամները, ռետինան և պերիֆերիկ նյարդերը։ Այսպիսով, թթվածնի դերը այս հիվանդությունում տեսանելի է ոչ միայն բջջային մակարդակում, այլ նաև համակարգային բարդությունների համատեքստում։
Նյարդային նեյրոդեգեներատիվ հիվանդություններ՝ ուղեղը ընդդեմ օքսիդացման
Ուղեղը օքսիդատիվ սթրեսի նկատմամբ ամենաառնչվող հյուսվածքներից է։ Նյարդային հյուսվածքում թթվածնի օգտագործումը շատ բարձր է, մինչդեռ նեյրոնները սահմանափակ բաժանման կարողություն ունեն։ Արդյունքում՝ կուտակված վնասը կարող է ունենալ անդառնալի հետևանքներ։
Ալցհեյմերի հիվանդության դեպքում ուղեղում հաղորդվել են լիպիդների և սպիտակուցների օքսիդացման բարձր նշաններ։ Պարկինսոնի հիվանդության դեպքում նկատվում է միտոխոնդրիալ դիսֆունկցիա և ROS-ի բարձրացում։ Այս պայմաններում անբնական սպիտակուցների կուտակումը կարող է լինել և պատճառ, և հետևանք օքսիդատիվ սթրեսի համար։
Ուղեղում թթվածինը կարևոր է, բայց պահանջում է հստակ կառավարում։ Ն—even փոքր խանգարումները ռեդոքս հավասարակշռության մեջ կարող են ազդել հիշողության, ճանաչողական ֆունկցիայի և նեյրոնալ գործունեության վրա։
Ռակ՝ ավելի բարդ երկիմաստություն
Ռակում ROS-ի հետ հարաբերությունը ավելի բարդ է։ Մի կողմից՝ DNA-ի օքսիդատիվ վնասը կարող է առաջացնել մուտացիաներ, որոնք սկսում են ուռուցքային գործընթացը։ Մյուս կողմից՝ շատ քաղցկեղային բջիջներ պահպանում են բարձր ROS մակարդակներ և պառադոքսալ կերպով օգտագործում դրանք proliferation-ի խթանման համար։
Այս բջիջները միաժամանակ ամրացնում են իրենց հակաօքսիդանտ համակարգերը, որպեսզի կանխեն չափազանց սթրեսից մահը։ Այս նուրբ հավասարակշռությունը դարձել է հակաքաղցկեղային թերապիաների հնարավոր թիրախ՝ քաղցկեղային բջիջներում ռեդոքս հոմեոստազը խաթարել, որպեսզի դրանք ընկնեն։
Թթվածնի թերապիա՝ օգուտի և ռիսկի սահմանը
Կլինիկական միջավայրում թթվածինը կենսական միջամտություն է՝ ինտենսիվ թերապիայի բաժանմունքներից մինչև թոքային հիվանդությունների բուժում և նույնիսկ հիպերբարիկ բժշկություն։ Այստեղ ևս կիրառվում է հավասարակշռության սկզբունքը։
Խիստ թթվածնի մատուցումը կարող է առաջացնել թթվածնի թունավորում՝ արտահայտված ROS-ի կտրուկ բարձրացմամբ, որը կարող է վնասել թոքային հյուսվածքը։ Այդ պատճառով ժամանակակից բժշկությունը շեշտադրում է թթվածնի հագեցվածության ճշգրիտ նպատակադրումը՝ պարզապես մակարդակները բարձրացնելու փոխարեն։
Սա ընդգծում է, որ թթվածինը պետք է օգտագործվի զգուշորեն, վերահսկված կերպով և համաչափ կենսաբանական անհրաժեշտությանը, լինի դա մարդկանց համար, թե արդյունաբերական կիրառություններում, որտեղ կարևոր են թթվածնի մաքրությունն ու մատակարարումը։
Մեթաբոլիզմ, ROS, տարիքը և տարիքի հետ կապված հիվանդություններ՝ հիմնական հարցը
Կարո՞ղ է այս գործընթացը լինել անխուսափելի։ Տարիքը միայն թթվածնի օգտագործման «գինն» է, թե՞ կարելի է մոդուլացնել կենսաբանական արձագանքը։
Ընթացիկ գիտությունը տալիս է պատասխան, որը ոչ լիովին կանխորոշված է, ոչ ամբողջովին օպտիմիստական։ Հստակ է, որ մարդկային մարմինը ստատիկ համակարգ չէ, այլ դինամիկ, հարմարվողական ցանց, որը կարող է բարձրացնել կամ նվազեցնել օքսիդատիվ սթրեսի կառավարման կարողությունը։
Վարժանք՝ ժամանակավոր ROS-ի աճ՝ պաշտպանական համակարգերի ամրապնդման համար
Սկզբում հակաբնական երևալով, վարժությունը, որը սովորաբար բարձրացնում է թթվածնի սպառումը, կարող է բարելավել ռեդոքս հավասարակշռությունը։ Ֆիզիկական ակտիվության ընթացքում մկաններում թթվածնի օգտագործումը աճում է՝ բարձրացնելով ROS արտադրությունը։ Սակայն, եթե այս աճը մնա ֆիզիոլոգիական սահմաններում, այն գործում է որպես հորմետիկ խթան։
Մեկուսացված ուսուցումը ակտիվացնում է Nrf2 ուղիները և բարձրացնում հակաօքսիդանտ էնզիմների արտահայտությունը։ Մարմինը արձագանքում է վարժությունից ստացած թեթև սթրեսին՝ բարձրացնելով պաշտպանական կարողությունը։ Սա բացատրում է, թե ինչու ֆիզիկապես ակտիվ մարդիկ, ընդհանուր առմամբ, ցածր օքսիդատիվ և բորբոքային նշաններ են ցուցաբերում։
Այս օրինակն ևս մեկ անգամ ցույց է տալիս, որ թթվածինը և ROS-ը բնազդաբար վնասակար չեն, այլ նրանց ազդեցությունը կախված է ինտենսիվությունից և ազդեցության ձևից։
Սնունդ՝ վառելիքի տեսակ և ռեդոքսի կարգավորում
Նյութափոխանակության վառելիքի որակը նույնպես ազդում է ROS-ի արտադրության վրա։ Պարզ շաքարների և մշակված ճարպերի բարձր պարունակությամբ դիետաները կարող են բարձրացնել օքսիդատիվ բեռը, մինչդեռ պոլիֆենոլներով, մանրաթելերով և օգտակար ճարպային թթուներով հարուստ դիետաները բարելավում են միտոխոնդրիալ ֆունկցիան։
Մոլեկուլներ, ինչպիսիք են ռեսվերատրոլը, կուրմինը և ֆլավոնոիդները, ոչ միայն ունեն անմիջական հակաօքսիդանտ հատկություններ, այլ նաև ակտիվացնում են երկար կյանքին կապված ազդանշանային ուղիները։ Ինչպես նշվել է նախկինում, նպատակը ոչ թե ամբողջությամբ վերացնել ROS-ը, այլ աջակցել մարմնի ներքին կարգավորող համակարգերին։
Քուն և ցիկլային ռիթմ
Տարիքի հետազոտության նոր տարածքներից է ցիկլային ռիթմի դերը նյութափոխանակության և ռեդոքսի կարգավորման մեջ։ Քնի խանգարումները կապված են օքսիդատիվ սթրեսի բարձր նշանների հետ։ Կանոնավոր քուն–արթնության ցիկլերը համակարգում են միտոխոնդրիալ գործունեությունը, DNA-ի վերականգնումը և վնասված մոլեկուլների հեռացումը։
Օքսիդատիվ սթրեսի մոնիտորինգի նոր տեխնոլոգիաներ
Բիոտեխնոլոգիայի առաջընթացը այժմ թույլ է տալիս չափել օքսիդատիվ նշանները արյան, միզի և հյուսվածքների մեջ։ Մոլեկուլներ՝ օրինակ՝ 8-oxo-dG, մալոնդիալդեհիդ և իսոպրոսթաներ, ծառայում են օքսիդատիվ վնասի ցուցիչների։
Ապագայում, կենսաբանական, գենետիկական և նյութափոխանակության տվյալների ինտեգրումը կարող է հնարավորություն տալ անհատականացված ռեդոքս պրոֆիլավորման՝ նպատակային միջամտությունների կիրառման համար տարիքային առողջության պահպանման գործում։
Թթվածնի արդյունաբերական–կենսաբանական տեսանկյունը
Թթվածնի արտադրությամբ, պահպանմամբ և մատակարարմամբ զբաղվող կազմակերպությունների համար կարևոր է հասկանալ այս կենսաբանական բարդությունը։ Թթվածինը պարզապես արդյունաբերական գազ չէ, այն կենսական բաղադրիչ է կենսաբժշկության, ինտենսիվ թերապիայի, բիոտեխնոլոգիայի և սննդի արդյունաբերության համար։
Թթվածնի մաքրության, ճնշման, չափաբաժնի և մատակարարման վերահսկումը բուժական կիրառություններում կարող է անմիջապես ազդել հյուսվածքային ռեդոքս հավասարակշռության վրա։ Արդյունքում, արդյունաբերական գազերի արտադրության որակը անուղղակիորեն կապված է բջջային առողջության հետ։
Մոլեկուլյար ուղիներ, որոնց միջոցով թթվածինը ազդում է տարիքի վրա
Մոլեկուլյար կենսաբանության տեսանկյունից տարիքայնացումը միայն բջջային կենցաղային տրավմայի արդյունք չէ։ Այն առաջանում է նյութափոխանակության ազդանշանների, բջջային էներգետիկ վիճակի, թթվածնի մակարդակների, ռեդոքս հավասարակշռության և գեների կարգավորման ցանցերի բարդ փոխազդեցությունից։ Թթվածինը գտնվում է այս ցանցի կենտրոնում։
1.Ազատ ռադիկալների տեսություն և դրա զարգացում
1950-ականներին Դենհեմ Հարմանը առաջարկեց Ազատ Ռադիկալների Տեսությունը՝ ենթադրելով, որ աէրոբ նյութափոխանակության ընթացքում արտադրվող ազատ ռադիկալները աստիճանաբար վնասում են կարևոր բջջային մոլեկուլները և այս կուտակված վնասը հանդիսանում է տարիքայնացման գլխավոր պատճառ։
Այսօր մենք հասկանում ենք, որ տեսությունը պետք է բարելավվի։ Խնդիրը միայն ROS-ի առկայությունը չէ, այլ դրանց արտադրության և հեռացման անհավասարակշռությունը։
- ROS-ի ցածր մակարդակները գործում են որպես ազդանշանային մոլեկուլներ։
- ROS-ի բարձր մակարդակները վնասարար են։
Այս մտածողության փոփոխությունը գիտնականներին հասցրեց կենտրոնանալ ոչ թե ROS-ի ամբողջական վերացման վրա, այլ ռեդոքս հոմեոստազի վրա։
Ռեդոքս հոմեոստազը բջջային օքսիդանտների և հակաօքսիդանտ համակարգերի հավասարակշռության պահպանումն է։ Երբ հավասարակշռությունը թեքվում է օքսիդանտների կողմը, առաջանում է օքսիդատիվ սթրես՝ կենսաբանական տարիքի նշան։
2.DNA-ի օքսիդատիվ վնաս և տարիքի հետ կապը
DNA-ն՝ կյանքի բլուպրինը, հանդիսանում է ROS-ի հիմնական թիրախ։ Օքսիդատիվ տեսակները, օրինակ՝ հիդրօքսիլ ռադիկալները, կարող են
- Օքսիդացնել նուկլեոտիդների հիմքերը (օրինակ՝ ձևավորել 8-oxo-dG)
- Գործել որպես DNA-ի միակի կամ երկակի շղթայի ճեղքումներ
- Հանդարտ replication համակարգի արդյունավետությունը
Չնայած բջիջները ունեն առաջադեմ DNA վերականգնման մեխանիզմներ (օրինակ՝ BER, NER, HR), դրանց արդյունավետությունը նվազում է տարիքի հետ։
3.Միտոխոնդրիա՝ ինչպես աղբյուր, այնպես էլ վնասի թիրախ
Միտոխոնդրիան, որպես թթվածնի օգտագործման հիմնական վայր, բնականաբար ենթարկվում է ամենաբարձր ROS մակարդակներին։
Միտոխոնդրիալ DNA-ն (mtDNA)՝
- Անհատուցելի է հիստոններով
- Սահմանափակ վերականգնման ունակություն ունի
- գտնվում է ROS-ի աղբյուրին մոտ
4.Թթվածին և mTOR ուղին
Մեկը կյանքի տևողության հիմնական կարգավորիչներից՝ mTOR (mammalian Target of Rapamycin) ուղին։
mTOR-ը զգայուն է էներգիայի, սննդանյութերի և աճի ազդանշանների նկատմամբ։ Երբ սննդանյութերը բավարար են, էներգիան բավարար է, և բջջային աճը ակտիվ է, mTOR-ը ակտիվանում է՝ խթանելով բջջային բաժանումը և սպիտակուցների սինթեզը։
Տարածվող mTOR ակտիվացումը կապվում է տարիքի և տարիքի հետ կապված հիվանդությունների հետ՝ ներառյալ քաղցկեղ, դիաբետ և նյարդաբանական հիվանդություններ։
Թթվածինը կարող է ազդել mTOR-ի ակտիվության վրա՝ ATP արտադրության և ռեդոքս վիճակի միջոցով, իսկ բարձր ROS մակարդակները կարող են փոփոխել ստորերկրյա կարգավորող ուղիները։ Հատկանշական է, որ mTOR արգելափակումը (օրինակ՝ ռապամիցինով) երկարացնում է կյանքի տևողությունը կենդանիների մոդելներում։
5.AMPK ուղի և նյութափոխանակության սթրեսին արձագանքը
AMPK-ը հակադիր է mTOR-ին և ակտիվանում է, երբ
- ATP-ի մակարդակը նվազում է
- AMP/ATP հարաբերակցությունը աճում է
- Բջիջները ենթարկվում են էներգետիկ սթրեսի
Թթվածինը անուղղակի կարգավորում է AMPK-ը ATP-ի արտադրության միջոցով։ Հիպոքսիայի դեպքում բջջային էներգետիկ վիճակի փոփոխությունը ակտիվացնում է պաշտպանական ուղիները։
6.HIF-1α՝ գենի մակարդակով թթվածնի սենսոր
HIF-1α-ն թթվածնի արձագանքի հիմնական կարգավորիչն է։
- Սովորական թթվածնի պայմաններում HIF-1α-ն արագ քայքայվում է
- Թթվածնի ցածր մակարդակի դեպքում HIF-1α-ն կայունանում է, տեղափոխվում է նուկլեուս և ինդուկցիա անում բջջային գոյատևման, անգիոգենեզի և գլիկոլիզի գեներում
Այս ուղու դիսրեգուլյացիան նպաստում է տարիքի և քաղցկեղի զարգացմանը։ Հետաքրքիր է, որ կարճաժամկետ վերահսկված հիպոքսիան կարող է inducել օգտակար հարմարվողական արձագանքներ (հորմեզ)։
7.Օքսիդատիվ հորմեզ՝ երբ սթրեսը դառնում է օգտակար
Հորմեզը նկարագրում է երևույթը, երբ ցածր մակարդակի սթրեսային գործոնը առաջացնում օգտակար հարմարվողական արձագանք։
————————————————–
ռեսուրս
Harman, D. (1956). Aging: A theory based on free radical and radiation chemistry. Journal of Gerontology.
López-Otín, C., Blasco, M.A., Partridge, L., Serrano, M., Kroemer, G. (2013). The hallmarks of aging. Cell.
Finkel, T., & Holbrook, N.J. (2000). Oxidants, oxidative stress and the biology of ageing. Nature.
Balaban, R.S., Nemoto, S., & Finkel, T. (2005). Mitochondria, oxidants, and aging. Cell.
Sena, L.A., & Chandel, N.S. (2012). Physiological roles of mitochondrial reactive oxygen species. Molecular Cell.
Ristow, M., & Schmeisser, S. (2014). Mitohormesis: Promoting health and lifespan by increased levels of reactive oxygen species (ROS). Dose-Response.