This post is also available in: English Armenian
اگر بخواهیم تنها یک عنصر را بهعنوان نماد حیات هوازی انتخاب کنیم، بیتردید اکسیژن در صدر فهرست قرار میگیرد. حدود ۲۱ درصد از اتمسفر زمین از اکسیژن تشکیل شده و این عنصر نقشی اساسی در شکلگیری تکامل زیستی داشته است. ورود اکسیژن به جو زمین در حدود ۲.۴ میلیارد سال پیش، طی رویدادی که به «انفجار بزرگ اکسیژن» معروف است، مسیر تکامل حیات را بهطور بنیادین تغییر داد. موجودات زندهای که توانستند از اکسیژن برای تولید انرژی استفاده کنند، بهدلیل بازده بالاتر متابولیسم هوازی نسبت به متابولیسم بیهوازی، مزیت تکاملی قابلتوجهی به دست آوردند.
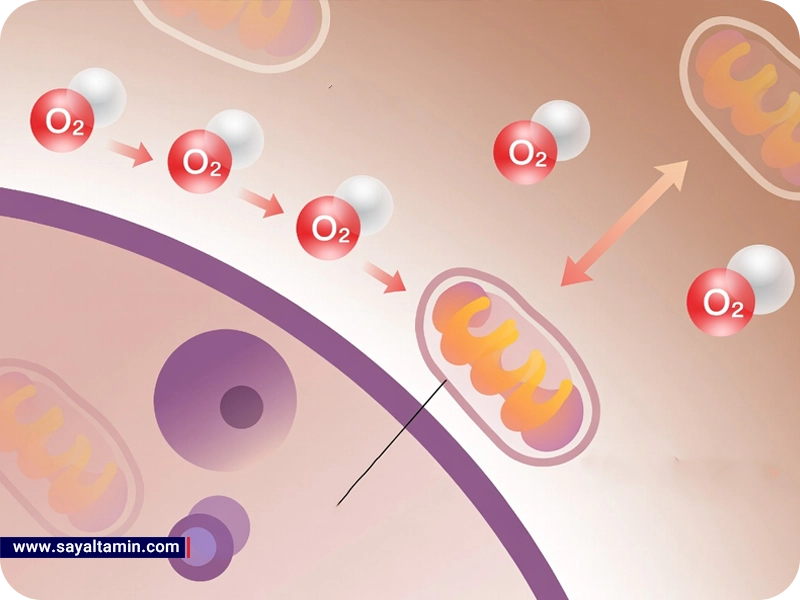
در انسان، تقریباً هر سلول برای ادامه حیات خود وابسته به اکسیژن است. قطع جریان اکسیژن برای چند دقیقه میتواند منجر به مرگ سلولی و آسیب برگشتناپذیر بافتی شود، بهویژه در بافتهایی با مصرف انرژی بالا مانند مغز و قلب. با این حال، همان اکسیژنی که برای بقا ضروری است، میتواند در سطح مولکولی به عامل تخریب تبدیل شود.
این پارادوکس زیستی، یعنی «اکسیژن بهعنوان منبع حیات و همزمان عامل آسیب»، یکی از جذابترین موضوعات در زیستشناسی سلولی و مولکولی است. درک این دوگانگی نهتنها برای علوم پزشکی و زیستفناوری اهمیت دارد، بلکه در حوزههای صنعتی مرتبط با تولید، ذخیرهسازی و انتقال اکسیژن نیز حائز اهمیت است؛ چرا که کیفیت، خلوص و کنترل اکسیژن در کاربردهای زیستی میتواند اثرات عمیقی بر سیستمهای زنده داشته باشد.
اکسیژن و متابولیسم سلولی: موتور انرژی حیات
۱. تنفس سلولی؛ از گلوکز تا ATP
برای درک نقش اکسیژن در متابولیسم، ابتدا باید مسیر تولید انرژی در سلول را بررسی کنیم. تنفس سلولی فرآیندی چندمرحلهای است که طی آن انرژی شیمیایی ذخیرهشده در مولکولهای آلی (مانند گلوکز) به ATP تبدیل میشود. این فرآیند شامل سه مرحله اصلی است:
– گلیکولیز (در سیتوزول)
– چرخه کربس یا چرخه اسید سیتریک (در ماتریکس میتوکندری)
– زنجیره انتقال الکترون و فسفریلاسیون اکسیداتیو (در غشای داخلی میتوکندری)
در دو مرحله نخست، الکترونهای پرانرژی از مولکولهای سوختی استخراج و به حاملهایی مانند NADH و FADH2 منتقل میشوند. اما مرحله سرنوشتساز در تولید انبوه ATP، زنجیره انتقال الکترون است؛ جایی که اکسیژن نقش محوری ایفا میکند.
۲. اکسیژن بهعنوان پذیرنده نهایی الکترون
در زنجیره انتقال الکترون، الکترونها از طریق مجموعهای از کمپلکسهای پروتئینی غشایی منتقل میشوند. در پایان این زنجیره، اکسیژن بهعنوان پذیرنده نهایی الکترون عمل کرده و با الکترونها و پروتونها ترکیب میشود تا مولکول آب را تشکیل دهد:
O₂ + 4e⁻ + 4H⁺ → 2H₂O
این واکنش ظاهراً ساده، در واقع ضامن بقای سلول است. اگر اکسیژن در دسترس نباشد، زنجیره انتقال الکترون متوقف شده و تولید ATP بهشدت کاهش مییابد. در چنین شرایطی، سلول به مسیرهای بیهوازی مانند تخمیر روی میآورد که بازده انرژی بسیار پایینتری دارند.
بهطور تقریبی، متابولیسم کامل یک مولکول گلوکز در حضور اکسیژن میتواند حدود ۳۰ تا ۳۲ مولکول ATP تولید کند، در حالی که در شرایط بیهوازی این عدد به ۲ ATP محدود میشود. همین تفاوت عظیم، اهمیت اکسیژن را در فیزیولوژی انسان نشان میدهد.
۳. میتوکندری؛ نیروگاه و منبع بالقوه آسیب
میتوکندری اغلب بهعنوان «نیروگاه سلول» شناخته میشود، اما این اندامک علاوه بر تولید انرژی، یکی از منابع اصلی تولید گونههای فعال اکسیژن نیز هست. در حالت طبیعی، حدود ۱ تا ۲ درصد از اکسیژن مصرفشده در زنجیره انتقال الکترون بهطور کامل به آب تبدیل نمیشود و به شکلهای ناقص احیاشده مانند سوپراکسید (O₂•⁻) درمیآید.
در شرایط فیزیولوژیک، این مقدار اندک ROS نهتنها مضر نیست، بلکه در تنظیم سیگنالینگ سلولی نقش دارد. اما اگر تولید ROS افزایش یابد یا سیستمهای دفاعی سلول تضعیف شوند، تعادل ظریف بین تولید و خنثیسازی به هم میخورد و استرس اکسیداتیو شکل میگیرد.
چهره دوم اکسیژن: از سیگنال زیستی تا استرس اکسیداتیو
اکسیژن مولکولی (O₂) در حالت پایه خود نسبتاً پایدار است. با این حال، ویژگی الکترونی خاص آن—یعنی وجود دو الکترون جفتنشده در اوربیتالهای مجزا—باعث میشود در شرایط خاص بهراحتی وارد واکنشهای ردوکس شود. این ویژگی همان چیزی است که امکان استخراج انرژی از سوختهای زیستی را فراهم میکند، اما همزمان زمینه تولید مشتقات واکنشپذیر و بالقوه مخرب را نیز مهیا میسازد.
در درون سلول، اکسیژن هرگز صرفاً یک گاز بیاثر نیست؛ بلکه در شبکهای پیچیده از تبادلات الکترونی مشارکت دارد. در این بستر پویا، بخشی از اکسیژن مصرفشده بهطور کامل به آب تبدیل نمیشود و به اشکالی نیمهاحیاشده درمیآید که به آنها «گونههای فعال اکسیژن» یا ROS گفته میشود.
ROS پیامد اجتنابناپذیر متابولیسم هوازی
تولید گونههای فعال اکسیژن را نباید یک خطای بیولوژیک تلقی کرد. در واقع، این پدیده پیامد طبیعی و اجتنابناپذیر استفاده از اکسیژن بهعنوان پذیرنده نهایی الکترون است. در میتوکندری، جایی که زنجیره انتقال الکترون با هدف تولید ATP فعالیت میکند، الکترونها از مجموعهای از کمپلکسهای پروتئینی عبور میکنند. این مسیر بسیار کارآمد است، اما صد درصد کامل نیست.
در جریان انتقال الکترون، درصد کوچکی از الکترونها پیش از رسیدن به انتهای زنجیره، با مولکولهای اکسیژن واکنش میدهند و سوپراکسید تولید میکنند. این رویداد در نگاه اول ناچیز به نظر میرسد—شاید تنها یک تا دو درصد از کل اکسیژن مصرفی—اما وقتی در نظر بگیریم که هر سلول بدن انسان روزانه میلیاردها مولکول اکسیژن مصرف میکند، این مقدار ناچیز به حجم قابلتوجهی از مولکولهای واکنشپذیر تبدیل میشود.
سوپراکسید میتواند به پراکسید هیدروژن تبدیل شود و در حضور یونهای فلزی مانند آهن، رادیکال هیدروکسیل شکل بگیرد؛ رادیکالی که از نظر شیمیایی یکی از مخربترین گونههای زیستی شناخته میشود. این زنجیره تبدیلها، نمونهای کلاسیک از این واقعیت است که متابولیسم هوازی ذاتاً با خطر همراه است.
نقش تنظیمی ROS؛ بازنگری در یک باور قدیمی
برای سالها، ROS صرفاً بهعنوان محصولات جانبی مضر متابولیسم تلقی میشدند. اما پژوهشهای دو دهه اخیر نشان دادهاند که این نگاه سادهانگارانه است. در حقیقت، سلولها از ROS بهعنوان مولکولهای سیگنالینگ استفاده میکنند.
پراکسید هیدروژن، برخلاف تصور عمومی، تنها یک عامل اکسیدکننده مخرب نیست؛ بلکه میتواند بهطور برگشتپذیر گروههای تیول در پروتئینها را اکسید کند و از این طریق فعالیت آنها را تنظیم نماید. بسیاری از مسیرهای پیامرسانی، از جمله مسیرهای مرتبط با رشد، تمایز، پاسخ به استرس و حتی تنظیم متابولیسم انرژی، به تغییرات ظریف در سطح ROS حساس هستند.
در واقع، میتوان گفت سلولها یاد گرفتهاند از «خطر کنترلشده» بهعنوان ابزار تنظیم استفاده کنند. این وضعیت را گاهی با اصطلاح «Redox Signaling» توصیف میکنند؛ حالتی که در آن تعادل اکسایش–کاهش به بخشی از زبان ارتباطی سلول تبدیل میشود.
اما همانطور که هر زبان تنظیمی نیازمند دقت است، در اینجا نیز مرز میان عملکرد مفید و آسیبزا بسیار باریک است.
زمانی که تعادل فرو میریزد: استرس اکسیداتیو
در یک سلول سالم، تولید ROS و خنثیسازی آنها در تعادل پویا قرار دارد. سیستمهای آنتیاکسیدانی آنزیمی و غیرآنزیمی دائماً در حال مهار گونههای فعال اکسیژن هستند. اما اگر به هر دلیل—افزایش مصرف انرژی، التهاب مزمن، آلودگی محیطی، اختلال میتوکندریایی یا کاهش کارایی سیستمهای دفاعی—این تعادل برهم بخورد، شرایطی ایجاد میشود که به آن «استرس اکسیداتیو» گفته میشود.
استرس اکسیداتیو صرفاً افزایش عددی ROS نیست؛ بلکه به معنای ناتوانی سیستم زیستی در مدیریت پیامدهای آن است. در این وضعیت، مولکولهای حیاتی سلول هدف واکنشهای اکسیداسیون قرار میگیرند.
لیپیدهای غشایی که غنی از اسیدهای چرب غیراشباع هستند، بهشدت مستعد حمله رادیکالها هستند. پراکسیداسیون لیپیدی میتواند ساختار و سیالیت غشا را تغییر دهد، کانالهای یونی را مختل کند و حتی پیامهای مرگ سلولی را فعال سازد. در بافتهایی مانند مغز که چگالی لیپیدی بالایی دارند، این آسیبها اهمیت دوچندان پیدا میکند.
پروتئینها نیز از این حملات در امان نیستند. اکسیداسیون میتواند ساختار سهبعدی آنها را تغییر دهد و آنها را از حالت عملکردی خارج کند. در برخی موارد، پروتئینهای آسیبدیده تجمع مییابند و ساختارهای نامحلول ایجاد میکنند؛ پدیدهای که در بیماریهای نورودژنراتیو مانند آلزایمر مشاهده میشود.
اما شاید مهمترین هدف ROS، ماده ژنتیکی باشد.
DNA؛ حافظهای در معرض اکسیداسیون
DNA، چه در هسته و چه در میتوکندری، بهطور مداوم در معرض حملات اکسیداتیو قرار دارد. تغییرات شیمیایی در بازهای نیتروژنی، شکستهای تکرشتهای و دورشتهای، و ایجاد جهشهای نقطهای از جمله پیامدهای این حملات هستند.
گرچه سلولها دارای سیستمهای ترمیم DNA هستند، اما این سیستمها کامل و بینقص نیستند. با گذشت زمان، بخشی از این آسیبها تجمع مییابد. این تجمع تدریجی، یکی از پایههای نظریههایی است که سالمندی را نتیجه انباشت آسیب مولکولی میدانند.
نکته قابلتوجه این است که DNA میتوکندریایی نسبت به DNA هستهای آسیبپذیرتر است. این DNA کوچک و حلقوی در نزدیکی محل اصلی تولید ROS قرار دارد و برخلاف DNA هستهای، از محافظت هیستونی گسترده برخوردار نیست. آسیب به mtDNA میتواند کارایی زنجیره انتقال الکترون را کاهش دهد، که خود به افزایش تولید ROS منجر میشود. این چرخه بازخوردی منفی، یکی از مدلهای پیشنهادی برای توضیح کاهش عملکرد سلولی با افزایش سن است.
جدول ۲ – طیف عملکردی ROS از تنظیم تا آسیب
| سطح ROS | وضعیت فیزیولوژیک | پیامد بیولوژیک |
| بسیار پایین | سیگنالینگ طبیعی | تنظیم رشد و تمایز |
| متوسط و کنترلشده | تعادل ردوکس پایدار | عملکرد طبیعی متابولیسم |
| بالا و پایدار | استرس اکسیداتیو | آسیب لیپیدی و پروتئینی |
| بسیار بالا | فروپاشی سلولی | فعالسازی آپوپتوز یا نکروز |
اکسیژن، التهاب و پیری سیستمیک
یکی از ابعاد پیچیدهتر ماجرا این است که ROS میتوانند مسیرهای التهابی را فعال کنند. فعالسازی مزمن فاکتورهای التهابی در سطح پایین، حالتی ایجاد میکند که برخی پژوهشگران آن را «التهاب وابسته به سن» یا inflammaging نامیدهاند.
در این وضعیت، بدن وارد چرخهای از تحریک مداوم سیستم ایمنی میشود. این التهاب خفیف اما پایدار میتواند زمینهساز بسیاری از بیماریهای وابسته به سن، از جمله بیماریهای قلبی–عروقی، دیابت نوع ۲ و اختلالات عصبی باشد.
به این ترتیب، اکسیژن نهتنها در سطح سلولی بلکه در سطح سیستمیک نیز در فرآیندهای مرتبط با سالمندی نقش ایفا میکند.
اکسیژن، استرس اکسیداتیو و نظریههای زیستی سالمندی
سالمندی؛ برنامهریزی ژنتیکی یا انباشت آسیب؟
سالمندی پدیدهای چندبعدی است که هنوز پاسخ نهایی و قطعی برای آن وجود ندارد. آیا پیری نتیجه یک برنامه ژنتیکی از پیش تعیینشده است؟ یا حاصل انباشت تدریجی آسیبهای مولکولی در طول زمان؟ در میان نظریههای متعدد مطرحشده، یکی از تأثیرگذارترین و ماندگارترین آنها «نظریه رادیکال آزاد سالمندی» است؛ نظریهای که مستقیماً به نقش دوگانه اکسیژن بازمیگردد.
در دهه ۱۹۵۰، دنهام هارمن پیشنهاد کرد که تولید مداوم رادیکالهای آزاد در طول متابولیسم هوازی، بهتدریج به اجزای سلولی آسیب وارد میکند و این آسیبهای تجمعی، بنیان زیستی سالمندی را تشکیل میدهند. این نظریه در زمان خود انقلابی بود، زیرا برای نخستین بار بین متابولیسم انرژی و فرآیند پیری پیوندی مستقیم برقرار کرد.
بر اساس این دیدگاه، هرچه یک ارگانیسم بیشتر از اکسیژن استفاده کند، میزان تولید رادیکالهای آزاد افزایش مییابد و در نتیجه سرعت انباشت آسیب بیشتر خواهد بود. به بیان سادهتر، «هزینه تنفس» همان هزینه زندگی است.
اما علم زیستشناسی هیچگاه در یک نقطه متوقف نمیشود.
بازنگری در نظریه رادیکال آزاد
در دهههای اخیر، دادههای تجربی پیچیدهتر از آن بودند که با نسخه ساده نظریه اولیه سازگار باشند. برخی موجودات با نرخ متابولیسم بالا، طول عمر زیادی دارند. برخی مدلهای حیوانی با افزایش سطح آنتیاکسیدانها، افزایش قابلتوجهی در طول عمر نشان ندادند. حتی در برخی موارد، افزایش خفیف ROS با افزایش طول عمر همراه بوده است.
این یافتهها نشان داد که ROS صرفاً «سموم تصادفی» نیستند، بلکه بخشی از شبکه تنظیمی حیاتاند. در نتیجه، نظریه کلاسیک رادیکال آزاد به نسخههای مدرنتری تکامل یافت که بر «اختلال در تعادل ردوکس» و «سیگنالینگ استرسی سازگارانه» تمرکز دارند.
یکی از مفاهیم کلیدی که در این بازنگری شکل گرفت، پدیدهای به نام «هورمزیس» (Hormesis) است.
هورمزیس؛ وقتی استرس خفیف مفید میشود
هورمزیس به حالتی اشاره دارد که در آن قرار گرفتن در معرض مقدار کم یک عامل استرسزا، موجب فعالسازی مسیرهای دفاعی و در نهایت افزایش مقاومت سلول میشود. در مورد اکسیژن، افزایش خفیف و کنترلشده ROS میتواند مسیرهای محافظتی را فعال کند.
برای مثال:
– فعالسازی فاکتور رونویسی Nrf2 که بیان ژنهای آنتیاکسیدانی را افزایش میدهد
– تحریک مسیرهای ترمیم DNA
– بهبود کارایی میتوکندری
به این ترتیب، مقدار کم ROS میتواند بهعنوان «سیگنال بیدارباش» عمل کند و سیستم دفاعی را تقویت نماید. اما اگر این استرس مزمن یا بیش از حد باشد، سیستم دفاعی فرسوده میشود و آسیب غالب میگردد.
این نگاه جدید نشان میدهد که رابطه اکسیژن و سالمندی خطی و ساده نیست؛ بلکه وابسته به شدت، مدت و زمینه زیستی است.
میتوکندری در مرکز معادله سالمندی
تقریباً تمامی مدلهای مدرن سالمندی، بهنوعی میتوکندری را در مرکز توجه قرار میدهند. دلیل این امر روشن است: میتوکندری هم منبع اصلی تولید انرژی و هم یکی از منابع اصلی ROS است.
با افزایش سن، چند تغییر کلیدی در میتوکندری مشاهده میشود:
– کاهش کارایی زنجیره انتقال الکترون
– افزایش نشت الکترونی
– تجمع جهش در DNA میتوکندریایی
– کاهش ظرفیت تولید ATP
این تغییرات میتوانند چرخهای معیوب ایجاد کنند: اختلال عملکرد میتوکندری → افزایش ROS → آسیب بیشتر → اختلال بیشتر.
با این حال، برخی مطالعات نشان دادهاند که افزایش خفیف ROS میتوکندریایی در مراحل اولیه زندگی میتواند مسیرهای طول عمر را فعال کند. این یافتهها نشان میدهد که کیفیت سیگنال اکسیداتیو، مهمتر از صرفاً مقدار آن است.
محدودیت کالری؛ کاهش مصرف اکسیژن یا بهینهسازی آن؟
یکی از قویترین مداخلاتی که در مدلهای حیوانی باعث افزایش طول عمر شده، محدودیت کالری بدون سوءتغذیه است. این پدیده از دهه ۱۹۳۰ مورد مطالعه قرار گرفته و در گونههای مختلف—from مخمر تا پستانداران—افزایش طول عمر را نشان داده است.
یکی از فرضیات اولیه این بود که محدودیت کالری با کاهش نرخ متابولیسم و مصرف اکسیژن، تولید ROS را کاهش میدهد. اما مطالعات دقیقتر نشان دادند که موضوع پیچیدهتر است.
محدودیت کالری مسیرهای مولکولی خاصی را فعال میکند، از جمله:
– Sirtuins (بهویژه SIRT1)
– AMPK
– مهار مسیر mTOR
این مسیرها در بهبود کارایی میتوکندری، افزایش اتوفاژی (پاکسازی اجزای آسیبدیده) و تقویت مقاومت سلولی نقش دارند. در واقع، به نظر میرسد محدودیت کالری نهتنها میزان مصرف اکسیژن را تنظیم میکند، بلکه نحوه استفاده از آن را بهینه میسازد.
به بیان دیگر، مسئله اصلی شاید «چقدر اکسیژن مصرف میکنیم» نباشد، بلکه «چگونه از آن استفاده میکنیم» باشد.
جدول ۳ – ارتباط مسیرهای مولکولی با اکسیژن و سالمندی
| مسیر مولکولی | ارتباط با ROS | تأثیر بر سالمندی |
| Nrf2 | فعالسازی توسط ROS خفیف | افزایش بیان ژنهای آنتیاکسیدانی |
| SIRT1 | وابسته به وضعیت انرژی | افزایش ترمیم DNA و کارایی میتوکندری |
| AMPK | حسگر انرژی | تحریک متابولیسم کارآمد |
| mTOR | حساس به مواد مغذی | مهار آن با افزایش طول عمر مرتبط است |
| p53 | پاسخ به آسیب DNA | تنظیم مرگ سلولی و پیری سلولی |
پیری سلولی (Cellular Senescence) و اکسیژن
یکی دیگر از جنبههای مهم ارتباط اکسیژن با سالمندی، پدیده «پیری سلولی» است. در این حالت، سلولها به دلیل آسیبهای تجمعی—از جمله آسیب اکسیداتیو—از چرخه تقسیم خارج میشوند اما زنده باقی میمانند. این سلولها معمولاً مجموعهای از مولکولهای التهابی ترشح میکنند که محیط بافتی را تغییر میدهد.
افزایش تعداد سلولهای پیر در بافتها یکی از ویژگیهای بارز افزایش سن است. استرس اکسیداتیو مزمن یکی از محرکهای اصلی ورود سلول به این وضعیت محسوب میشود.
سیستمهای دفاع آنتیاکسیدانی و حفظ تعادل ردوکس
چگونه سلول با اکسیژن زندگی میکند بدون آنکه در آن بسوزد؟
اگر اکسیژن را آتشی کنترلشده بدانیم که موتور زندگی را روشن نگه میدارد، سیستمهای آنتیاکسیدانی همان مهندسی دقیقی هستند که اجازه نمیدهند این آتش به حریق تبدیل شود. حیات هوازی بدون این سامانههای حفاظتی اساساً ممکن نبود. در واقع، تکامل موجودات چندسلولی همزمان با تکامل مکانیسمهایی بوده که بتوانند انرژی حاصل از اکسیداسیون را مهار و مدیریت کنند.
سلول در هر لحظه در حال تجربه تبادلات اکسایش–کاهش (ردوکس) است. این تبادلات نهتنها در میتوکندری، بلکه در سیتوزول، هسته، شبکه آندوپلاسمی و حتی غشای پلاسمایی رخ میدهند. بنابراین، حفظ تعادل ردوکس یک فرآیند موضعی و لحظهای است، نه یک وضعیت ثابت.
دفاع خط اول: آنزیمهای آنتیاکسیدانی
در قلب سیستم دفاعی سلول، آنزیمهایی قرار دارند که بهصورت تخصصی برای خنثیسازی ROS طراحی شدهاند. این آنزیمها نهتنها سرعت واکنش بالایی دارند، بلکه در مکانهای استراتژیک سلول مستقر هستند.
سوپراکسید دیسموتاز (SOD) یکی از اولین سدهای دفاعی در برابر سوپراکسید است. این آنزیم، سوپراکسید را به پراکسید هیدروژن تبدیل میکند؛ مولکولی که اگرچه هنوز واکنشپذیر است، اما از سوپراکسید پایدارتر و قابلکنترلتر است. جالب آنکه سلول چندین نوع SOD دارد: نوع سیتوزولی، نوع میتوکندریایی و حتی نوع خارجسلولی. این تنوع نشان میدهد که مدیریت ROS در هر بخش سلول اهمیت دارد.
پراکسید هیدروژن حاصل، سپس توسط آنزیمهایی مانند کاتالاز و گلوتاتیون پراکسیداز تجزیه میشود. کاتالاز آن را مستقیماً به آب و اکسیژن تبدیل میکند، در حالی که گلوتاتیون پراکسیداز با استفاده از مولکولی به نام گلوتاتیون، پراکسید هیدروژن را به آب کاهش میدهد.
این زنجیره دفاعی نشان میدهد که بدن نهتنها ROS را حذف میکند، بلکه آنها را بهصورت مرحلهای و کنترلشده مدیریت میکند.
گلوتاتیون؛ ستون تعادل ردوکس
در میان تمام مولکولهای آنتیاکسیدانی، گلوتاتیون جایگاه ویژهای دارد. این تریپپتید کوچک، یکی از فراوانترین آنتیاکسیدانهای درونسلولی است و نقش آن فراتر از یک خنثیکننده ساده ROS است.
گلوتاتیون در دو حالت احیاشده (GSH) و اکسیدشده (GSSG) وجود دارد. نسبت این دو شکل، یکی از شاخصهای اصلی وضعیت ردوکس سلول محسوب میشود. زمانی که ROS افزایش مییابد، گلوتاتیون احیاشده مصرف میشود. اگر سلول نتواند آن را مجدداً احیا کند، تعادل بهسمت استرس اکسیداتیو سوق پیدا میکند.
با افزایش سن، مطالعات نشان دادهاند که سطح گلوتاتیون در بسیاری از بافتها کاهش مییابد. این کاهش میتواند یکی از دلایل افزایش حساسیت به آسیب اکسیداتیو در سالمندان باشد.
چرا مکملهای آنتیاکسیدانی همیشه معجزه نمیکنند؟
در دهههای گذشته، تصور میشد که مصرف مکملهای آنتیاکسیدانی مانند ویتامین C، ویتامین E یا بتاکاروتن میتواند روند سالمندی را کند کند. اما نتایج کارآزماییهای بالینی بزرگ، تصویر پیچیدهتری ارائه دادند.
در بسیاری از مطالعات، مصرف دوزهای بالای آنتیاکسیدان نهتنها طول عمر را افزایش نداد، بلکه در برخی موارد با افزایش خطر برخی بیماریها همراه بود. دلیل این تناقض چیست؟
پاسخ در همان مفهوم هورمزیس نهفته است. اگر ROS در سطوح پایین نقش سیگنالینگ دارند، حذف بیشازحد آنها میتواند مسیرهای سازگارانه را مختل کند. بدن برای حفظ تعادل ردوکس به یک سطح مشخص از فعالیت اکسیداتیو نیاز دارد. سرکوب کامل آن نه ممکن است و نه مطلوب.
این یافتهها نشان میدهد که مسئله اصلی در زیستشناسی سالمندی، «حذف اکسیژن» یا «حذف ROS» نیست، بلکه حفظ تعادل پویا میان تولید و خنثیسازی است.
Redox Homeostasis مفهوم مرکزی در پیری
اصطلاح Redox Homeostasis به تعادل دینامیک میان واکنشهای اکسایش و کاهش در سلول اشاره دارد. این تعادل، شبیه یک ترموستات زیستی عمل میکند. نه اکسیداسیون بیش از حد مطلوب است و نه کاهش بیش از حد.
با افزایش سن، این ترموستات زیستی دچار نوسان میشود. کارایی میتوکندری کاهش مییابد، سیستمهای ترمیمی ضعیفتر میشوند، سطح گلوتاتیون کاهش پیدا میکند و پاسخهای التهابی افزایش مییابد. نتیجه این تغییرات، انتقال تدریجی سیستم به سمت یک وضعیت اکسیداتیو مزمن است.
در این مرحله، اکسیژن همچنان برای حیات ضروری است، اما ظرفیت سیستم برای مدیریت پیامدهای آن کاهش یافته است. به همین دلیل است که بیماریهای وابسته به سن اغلب با نشانگرهای افزایشیافته استرس اکسیداتیو همراهاند.
استرس اکسیداتیو، اکسیژن و بیماریهای وابسته به سن
وقتی تعادل ردوکس در مقیاس بافت و ارگانیسم مختل میشود
تا اینجا اکسیژن را در مقیاس سلولی بررسی کردیم؛ در میتوکندری، در DNA، در شبکههای سیگنالینگ و در سیستمهای دفاعی. اما پیامدهای اختلال در تعادل اکسیداسیون–کاهش تنها به یک سلول محدود نمیماند. با افزایش سن، تغییرات تجمعی در میلیونها میلیارد سلول، خود را در سطح بافتها و اندامها نشان میدهد. در این مرحله است که استرس اکسیداتیو به یک پدیده سیستمیک تبدیل میشود.
افزایش مزمن گونههای فعال اکسیژن، همراه با کاهش تدریجی کارایی سیستمهای دفاعی، بستری ایجاد میکند که بسیاری از بیماریهای وابسته به سن در آن شکل میگیرند. این بیماریها لزوماً بهدلیل «زیاد بودن اکسیژن» ایجاد نمیشوند، بلکه بهدلیل ناتوانی سیستم زیستی در مدیریت تبعات مصرف مداوم آن بروز میکنند.
بیماریهای قلبی–عروقی؛ اکسیداسیون در دیواره عروق
یکی از شناختهشدهترین نمونههای ارتباط استرس اکسیداتیو با بیماری، آترواسکلروز است. در این بیماری، لیپوپروتئینهای کمچگال (LDL) در دیواره عروق اکسید میشوند. LDL اکسیدشده توسط سلولهای ایمنی شناسایی و بلعیده میشود و در نهایت به تشکیل «پلاک» در دیواره رگ منجر میگردد.
گونههای فعال اکسیژن در این فرآیند نقش کلیدی دارند. آنها هم در اکسیداسیون LDL دخیلاند و هم مسیرهای التهابی را فعال میکنند. نتیجه نهایی، کاهش انعطافپذیری عروق، تنگی رگها و افزایش خطر سکته قلبی یا مغزی است.
با افزایش سن، عملکرد سلولهای اندوتلیال (پوشش داخلی عروق) نیز تحت تأثیر استرس اکسیداتیو قرار میگیرد. تولید نیتریک اکسید—مولکولی که باعث اتساع عروق میشود—کاهش مییابد و در نتیجه تنظیم فشار خون مختل میشود. به این ترتیب، اکسیژن از طریق واسطههای اکسیداتیو، در قلب یکی از مهمترین چالشهای سلامت سالمندان قرار میگیرد.
دیابت نوع ۲؛ چرخه معیوب متابولیسم و ROS
در دیابت نوع ۲، مقاومت به انسولین و اختلال در متابولیسم گلوکز با افزایش تولید ROS همراه است. قند خون بالا موجب افزایش جریان الکترون در زنجیره انتقال الکترون میشود و این موضوع نشت الکترونی را تشدید میکند. در نتیجه، تولید سوپراکسید افزایش مییابد.
ROS به نوبه خود مسیرهای التهابی و اختلال در سیگنالینگ انسولین را تقویت میکنند. این وضعیت یک چرخه معیوب ایجاد میکند: هایپرگلیسمی → افزایش ROS → تشدید مقاومت به انسولین → افزایش بیشتر قند خون.
در بلندمدت، استرس اکسیداتیو در دیابت با آسیب به عروق کوچک (میکروآنژیوپاتی)، کلیهها، شبکیه و اعصاب محیطی همراه است. بنابراین، نقش اکسیژن در این بیماری نهتنها در سطح سلولی، بلکه در عوارض سیستمیک نیز آشکار است.
بیماریهای نورودژنراتیو؛ مغز در برابر اکسیداسیون
مغز یکی از حساسترین بافتها نسبت به استرس اکسیداتیو است. مصرف اکسیژن در بافت عصبی بسیار بالاست و در عین حال، نورونها ظرفیت تقسیم محدودی دارند. به همین دلیل، آسیب تجمعی در آنها میتواند پیامدهای جبرانناپذیر داشته باشد.
در بیماری آلزایمر، افزایش نشانگرهای اکسیداسیون لیپیدی و پروتئینی در بافت مغز گزارش شده است. در پارکینسون نیز اختلال در عملکرد میتوکندری و افزایش ROS مشاهده میشود. تجمع پروتئینهای غیرطبیعی در این بیماریها میتواند هم علت و هم معلول استرس اکسیداتیو باشد.
اکسیژن در مغز همانقدر که حیاتی است، به همان اندازه نیازمند مدیریت دقیق است. کوچکترین اختلال در تعادل ردوکس میتواند بر حافظه، شناخت و عملکرد عصبی اثر بگذارد.
سرطان؛ دوگانگی پیچیدهتر
در سرطان، رابطه با ROS پیچیدهتر است. از یک سو، آسیب اکسیداتیو به DNA میتواند جهشهایی ایجاد کند که آغازگر سرطان باشند. از سوی دیگر، بسیاری از سلولهای سرطانی سطح بالاتری از ROS دارند و بهطور پارادوکسیکال از آن برای تحریک تکثیر استفاده میکنند.
با این حال، این سلولها بهطور همزمان سیستمهای آنتیاکسیدانی خود را نیز تقویت میکنند تا از مرگ ناشی از استرس شدید جلوگیری کنند. این تعادل ظریف، امروزه بهعنوان یکی از اهداف بالقوه درمانهای ضدسرطان مورد توجه قرار گرفته است؛ یعنی برهم زدن تعادل ردوکس در سلول سرطانی بهگونهای که به سمت فروپاشی سوق داده شود.
اکسیژن درمانی؛ مرز میان سود و خطر
در محیطهای درمانی، اکسیژن بهعنوان یک مداخله حیاتی استفاده میشود؛ از بخشهای مراقبت ویژه گرفته تا درمان بیماریهای ریوی و حتی پزشکی هایپرباریک. اما در اینجا نیز اصل تعادل مطرح است.
تجویز بیش از حد اکسیژن میتواند به «سمیت اکسیژن» منجر شود، حالتی که با افزایش شدید تولید ROS همراه است و ممکن است به بافت ریه آسیب برساند. به همین دلیل، در پزشکی مدرن تأکید بر «هدفگذاری دقیق سطح اشباع اکسیژن» است، نه صرفاً افزایش آن.
این موضوع بار دیگر نشان میدهد که اکسیژن باید دقیق، کنترلشده و متناسب با نیاز زیستی استفاده شود؛ چه در بدن انسان و چه در کاربردهای صنعتی مرتبط با تأمین و خلوص آن.
پس از بررسی نقش اکسیژن در متابولیسم، تولید ROS، سالمندی و بیماریهای وابسته به سن، اکنون پرسش کلیدی این است: آیا این فرآیند اجتنابناپذیر است؟ آیا سالمندی صرفاً بهای مصرف اکسیژن است، یا میتوان نحوه مواجهه زیستی با آن را تغییر داد؟
پاسخ علم امروز، نه کاملاً جبرگرایانه است و نه کاملاً خوشبینانه. آنچه روشن است، این است که بدن انسان یک سامانه ایستا نیست؛ بلکه شبکهای پویا و سازگار است که میتواند ظرفیت مدیریت استرس اکسیداتیو خود را افزایش یا کاهش دهد.
ورزش؛ افزایش موقت ROS برای تقویت سیستم دفاعی
شاید در نگاه اول عجیب به نظر برسد، اما ورزش—که معمولاً با افزایش مصرف اکسیژن همراه است—میتواند به بهبود تعادل ردوکس کمک کند. در حین فعالیت بدنی، مصرف اکسیژن در عضلات افزایش مییابد و به تبع آن تولید ROS نیز بیشتر میشود. اما این افزایش، اگر در حد فیزیولوژیک باشد، نقش هورمزیس را ایفا میکند.
تمرین منظم موجب فعالسازی مسیرهایی مانند Nrf2 و افزایش بیان آنزیمهای آنتیاکسیدانی میشود. در واقع، بدن در پاسخ به استرس خفیف ناشی از ورزش، ظرفیت دفاعی خود را ارتقا میدهد. به همین دلیل است که افراد دارای فعالیت بدنی منظم معمولاً نشانگرهای التهابی و اکسیداتیو پایینتری دارند.
این مثال بار دیگر نشان میدهد که اکسیژن و ROS ذاتاً دشمن نیستند؛ بلکه شدت و الگوی مواجهه با آنها تعیینکننده است.
تغذیه؛ تنظیم سوخت و وضعیت ردوکس
نوع و کیفیت سوخت متابولیکی نیز بر تولید ROS اثرگذار است. رژیمهای غذایی سرشار از قندهای ساده و چربیهای فرآوریشده میتوانند بار اکسیداتیو را افزایش دهند، در حالی که رژیمهای غنی از ترکیبات پلیفنولی، فیبر و اسیدهای چرب مفید با بهبود عملکرد میتوکندری همراه هستند.
ترکیباتی مانند رزوراترول، کورکومین و فلاونوئیدها نهتنها خاصیت آنتیاکسیدانی مستقیم دارند، بلکه مسیرهای سیگنالینگ مرتبط با طول عمر را نیز فعال میکنند. با این حال، همانطور که پیشتر اشاره شد، هدف حذف کامل ROS نیست، بلکه حمایت از سیستمهای تنظیمی درونی بدن است.
خواب و ریتم شبانهروزی
یکی از حوزههای نوظهور در ارتباط با سالمندی، نقش ریتم شبانهروزی در تنظیم متابولیسم و وضعیت ردوکس است. اختلال در خواب با افزایش نشانگرهای استرس اکسیداتیو همراه است. چرخههای منظم خواب–بیداری به هماهنگی فعالیت میتوکندری، ترمیم DNA و پاکسازی مولکولهای آسیبدیده کمک میکنند.
فناوریهای نوین در پایش استرس اکسیداتیو
با پیشرفت فناوریهای زیستی، امکان اندازهگیری نشانگرهای اکسیداتیو در خون، ادرار و بافتها فراهم شده است. مولکولهایی مانند 8-oxo-dG، مالوندیآلدئید و ایزوپروستانها بهعنوان شاخصهای آسیب اکسیداتیو مورد استفاده قرار میگیرند.
در آینده، ترکیب دادههای زیستی، ژنتیکی و متابولیکی میتواند به ایجاد پروفایلهای شخصیشده ردوکس منجر شود؛ رویکردی که شاید امکان مداخلات دقیقتر برای حفظ سلامت در دوران سالمندی را فراهم کند.
نگاه صنعتی–زیستی به اکسیژن
برای مجموعههایی که در حوزه تولید، ذخیرهسازی و تأمین اکسیژن فعالیت میکنند، درک این پیچیدگی زیستی اهمیت مضاعف دارد. اکسیژن تنها یک گاز صنعتی نیست؛ بلکه مولفهای حیاتی در زیستپزشکی، مراقبتهای ویژه، فناوریهای زیستی و صنایع غذایی است.
کنترل خلوص، فشار، دوز و نحوه انتقال اکسیژن در کاربردهای درمانی میتواند پیامدهای مستقیم بر تعادل ردوکس بافتها داشته باشد. بنابراین، کیفیت مهندسی در حوزه گازهای صنعتی بهطور غیرمستقیم با سلامت سلولی پیوند میخورد.
مسیرهای مولکولی که اکسیژن از طریق آنها سالمندی را شکل میدهد
اگر بخواهیم از نگاه یک زیستشناس مولکولی به موضوع نگاه کنیم، سالمندی صرفاً نتیجه «فرسودگی ساده» سلولها نیست. بلکه حاصل تعامل پیچیدهای میان سیگنالهای متابولیکی، وضعیت انرژی سلول، سطح اکسیژن، تعادل اکسید–احیا و شبکههای تنظیم ژن است. در این میان، اکسیژن در مرکز این شبکه قرار دارد.
۱. نظریه رادیکال آزاد و تکامل آن
در دهه ۱۹۵۰، دنهام هارمن «نظریه رادیکال آزاد سالمندی» را مطرح کرد. بر اساس این نظریه، رادیکالهای آزاد تولیدشده در طی متابولیسم هوازی بهتدریج به مولکولهای حیاتی سلول آسیب میزنند و این آسیب تجمعی عامل اصلی پیری است.
امروزه میدانیم که این نظریه نیاز به اصلاح دارد. مشکل صرفاً «وجود ROS» نیست؛ بلکه عدم تعادل بین تولید و حذف آنها اهمیت دارد. در واقع:
– ROS در سطح پایین، نقش سیگنالدهنده دارند.
– ROS در سطح بالا، مخرب هستند.
این تحول فکری باعث شد دانشمندان به جای تمرکز صرف بر «حذف کامل ROS»، به مفهوم «هومئوستاز ردوکس» توجه کنند.
هومئوستاز ردوکس یعنی حفظ تعادل میان گونههای اکسیدکننده و سیستمهای آنتیاکسیدانی سلول.
وقتی این تعادل به نفع اکسیدکنندهها تغییر کند، استرس اکسیداتیو رخ میدهد؛ وضعیتی که یکی از مشخصههای اصلی سالمندی زیستی محسوب میشود.
۲. آسیب اکسیداتیو به DNA و ارتباط آن با پیری
DNA به عنوان کتابچه راهنمای حیات، هدف مهم ROS است. گونههایی مانند رادیکال هیدروکسیل میتوانند:
– بازهای نوکلئوتیدی را اکسید کنند (مثلاً تشکیل 8-oxo-dG)
– باعث شکست تکرشتهای یا دورشتهای DNA شوند
– کارایی سیستمهای همانندسازی را مختل کنند
اگرچه سلول دارای سیستمهای ترمیم DNA بسیار پیشرفتهای است (مانند BER، NER و HR)، اما با افزایش سن کارایی این سیستمها کاهش مییابد.
۳. میتوکندری: هم منبع آسیب، هم هدف آسیب
میتوکندری به دلیل اینکه محل اصلی مصرف اکسیژن است، بهطور طبیعی در معرض بیشترین تولید ROS قرار دارد.
DNA میتوکندری (mtDNA) برخلاف DNA هسته:
– فاقد هیستونهای محافظتی است
– سیستم ترمیم محدودتری دارد
– در نزدیکی منبع ROS قرار گرفته است
۴. اکسیژن و مسیر mTOR
یکی از مهمترین مسیرهای تنظیم طول عمر، مسیر mTOR (mammalian Target of Rapamycin) است.
mTOR حسگر وضعیت انرژی، مواد مغذی و سیگنالهای رشد است. زمانی که:
– مواد مغذی فراواناند
– انرژی کافی وجود دارد
– رشد سلولی فعال است
mTOR فعال میشود و تقسیم و سنتز پروتئین را افزایش میدهد.
اما فعالبودن مزمن mTOR با پیری و بیماریهای مرتبط با سن (مانند سرطان، دیابت و بیماریهای نورودژنراتیو) مرتبط است.
اکسیژن از طریق تنظیم تولید ATP و وضعیت ردوکس، میتواند فعالیت mTOR را تحت تأثیر قرار دهد. همچنین ROS بالا قادر است مسیرهای تنظیمی پاییندستی mTOR را تغییر دهد.
جالب است بدانیم که مهار mTOR (مثلاً با داروی راپامایسین) در مدلهای حیوانی باعث افزایش طول عمر شده است.
۵. مسیر AMPK و پاسخ به استرس متابولیکی
در نقطه مقابل mTOR، مسیر AMPK قرار دارد.
AMPK زمانی فعال میشود که:
– سطح ATP کاهش یابد
– نسبت AMP به ATP افزایش پیدا کند
– سلول در وضعیت استرس انرژی قرار گیرد
اکسیژن از طریق تأثیر بر تولید ATP، بهطور غیرمستقیم فعالیت AMPK را تنظیم میکند. در شرایط کماکسیژنی (Hypoxia)، تغییر در وضعیت انرژی سلول باعث فعال شدن مسیرهای حفاظتی میشود.
۶. HIF-1α: سنسور اکسیژن در سطح ژنی
یکی از مهمترین تنظیمکنندههای پاسخ به اکسیژن، فاکتور HIF-1α است.
در شرایط نرمال اکسیژن:
– HIF-1α سریعاً تخریب میشود.
درشرایط کماکسیژنی:
– HIF-1α پایدار میشود.
– وارد هسته میشود.
– بیان ژنهای مرتبط با بقا، آنژیوژنز و گلیکولیز را افزایش میدهد.
تنظیم نادرست این مسیر در پیری و سرطان نقش دارد.
جالب اینکه برخی مطالعات نشان دادهاند قرار گرفتن کوتاهمدت در شرایط هیپوکسی کنترلشده میتواند پاسخهای تطبیقی مفیدی ایجاد کند (پدیده Hormesis).
۷. هورمسیس اکسیداتیو: وقتی استرس مفید میشود
هورمسیس به پدیدهای گفته میشود که در آن مقدار کم یک عامل استرسزا، پاسخ تطبیقی مفیدی ایجاد میکند.
————————————————–
منابع
Harman, D. (1956). Aging: A theory based on free radical and radiation chemistry. Journal of Gerontology.
López-Otín, C., Blasco, M.A., Partridge, L., Serrano, M., Kroemer, G. (2013). The hallmarks of aging. Cell.
Finkel, T., & Holbrook, N.J. (2000). Oxidants, oxidative stress and the biology of ageing. Nature.
Balaban, R.S., Nemoto, S., & Finkel, T. (2005). Mitochondria, oxidants, and aging. Cell.
Sena, L.A., & Chandel, N.S. (2012). Physiological roles of mitochondrial reactive oxygen species. Molecular Cell.
Ristow, M., & Schmeisser, S. (2014). Mitohormesis: Promoting health and lifespan by increased levels of reactive oxygen species (ROS). Dose-Response.